Месяц: Апрель 2020
ЛИТИЙ ГИДРОКСИД МОНОГИДРАТ
Литий гидроокись моногидрат – белый порошок с бесцветными кристаллами. Кристаллическая решетка тетрагональная.
СВОЙСТВА
Литий гидроксид — неорганическое основание щелочного металла лития, имеющее формулу LiOH. Является сильным основанием, но наиболее слабым основанием среди щелочных металлов.
Гидроксид лития при стандартных условиях представляет собой бесцветные кристаллы с тетрагональной решёткой. Бесцветный или белый порошок, без запаха. Гигроскопичен. Растворим в воде. При взаимодействии с водой возможен разогрев. Нелетуч. Коррозионен для некоторых металлов. На воздухе поглощает углекислый газ и образует углекислый литий, токсичность которого определяется наличием лития.
Приготовляют насыщенные растворы из эквивалентных количеств сульфата лития Li2SO4 и гидроксида бария Ba(OH)2. Затем растворы смешивают и выпавший осадок сульфата бария отфильтровывают. Фильтрат испытывают в отдельной пробе на полноту взаимодействия, т. е. на сульфат-ионы. При наличии непрореагировавшего сульфата лития к фильтрату прибавляют небольшое количество (несколько капель) раствора гидроксида бария. Осадок снова отфильтровывают. Если же был прилит избыток гидроксида бария (узнается в отдельной пробе реакцией на ион бария), то к фильтрату прибавляют небольшое количество сульфата лития. Фильтрат выпаривают в платиновой чашке в вакууме. Гидроксид лития дает пересыщенные растворы, и иногда только через несколько дней из раствора выпадают бесцветные игольчатые кристаллы моногидрата LiOH•H2O. При температуре выше 140°C он теряет воду. Гидроксид лития получается в виде белой полупрозрачной массы; на воздухе он постепенно притягивает влагу и реагирует с оксидом углерода (IV). Хранить его нужно в плотно закрытых склянках или в запаянных ампулах.
ПРИМЕНЕНИЕ
Гидроокись лития LiOH*H2O применяется:
— при изготовлении электролита для аккумуляторов;
— при изготовлении смазочных материалов, обладающих высокой стабильностью механических показателей при значительном изменении температуры (от –60°C до 160°C);
— в химической промышленности, как реагент для получения соединений Li, в частности олеатов, стеаратов и пальмитатов;
— для очистки и кондиционирования воздуха, как поглотитель СО2 в противогазах, подводных лодках, самолетах и космических кораблях;
— в стекольной и керамической промышленности;
— в радиотехнике.
ПОКАЗАТЕЛИ
| Наименование | Показатель |
| Массовая доля основного вещества, %, не менее | 56,5 |
| Массовая доля СО2, %, не более | 0,35 |
| Массовая доля SO4, %, не более | 0,05 |
| Массовая доля Cl, %, не более | 0,02 |
| Массовая доля NaOH, %, не более | 0,05 |
| Массовая доля CaO, %, не более | 0,03 |
| Массовая доля Fe2O3, %, не более | 0,003 |
| Вещества не растворимые в HCl, % | 0,01 |
КАЛЬЦИЙ ГИДРОКСИД
Кальций гидроксид — неорганическое соединение, щелочь кальция. Представляет собой мелкокристаллический порошок белого цвета, малорастворимый в воде.
СВОЙСТВА
Некоторые распространённые названия:
Пушенка — тонкоизмельченный порошок. Известковое молоко — водная взвесь щелочи, непрозрачная белая жидкость. Известковая вода — прозрачный водный раствор щелочи, получается после фильтрации известкового молока.
Гашеная известь получила название по способу получения: негашеную известь (оксид кальция) заливают водой (гасят).
Мелкий кристаллический порошок белого цвета, без запаха. Очень плохо растворяется в воде, совсем не растворяется в спирте, легко растворяется в разбавленной азотной и соляной кислотах. Пожаробезопасен и даже препятствует возгоранию. При нагревании разлагается на воду и оксид кальция.
Сильная щелочь. Вступает в реакции нейтрализации с кислотами с образованием солей — карбонатов. При взаимодействии с металлами выделяется взрывоопасный и горючий водород. Вступает в реакции с оксидами углерода (IV) и (II), с солями.
Реакция получения гидроокиси кальция методом «гашения» происходит с большим выделением тепла, вода начинает кипеть, едкий раствор разбрызгивается в разные стороны — это надо учитывать при работе.
Попадание на кожу частиц сухого порошка или капель раствора гидроокиси кальция вызывает раздражение, зуд, химический ожог, язвы, сильную боль. Повреждение глаз может вызвать потерю зрения. Проглатывание вещества вызывает ожог слизистой горла, рвоту, кровавую диарею, резкое снижение давления, повреждение внутренних органов. Вдыхание частиц пыли может привести к затрудняющей дыхание опухоли горла.
Работать с гидроокисью кальция следует в хорошо проветриваемых помещениях с применением средств защиты: резиновых перчаток, защитных очков и респираторов. Химические эксперименты должны проводиться в вытяжном шкафу.
ПРИМЕНЕНИЕ
— В строительной индустрии хим.реактив добавляют в связывающие растворы, штукатурку, белила, гипсовые растворы; на его основе изготавливают силикатный кирпич и бетон; с его помощью подготавливают почву перед укладкой дорожных покрытий. Побелка деревянных деталей конструкций и заборов придает им огнестойкие свойства и защищает от гниения.
— Для нейтрализации кислотных газов в металлургии.
— Для получения твердых масел и добавок к маслам — в нефтеперерабатывающей отрасли.
— В химической промышленности — для производства щелочей натрия и калия, хлорной извести («хлорки»), стеарата кальция, органических кислот.
— В аналитической химии известковая вода служит индикатором углекислого газа (поглощая его, она мутнеет).
— С помощью гидроокиси кальция очищают сточные и промышленные воды; нейтрализуют кислоты поступающей в водопроводы воды, чтобы снизить ее коррозионное воздействие; удаляют из воды карбонаты (умягчают воду).
— С помощью Ca(OH)2 удаляют волосяной покров со шкур в кожевенном деле.
— Пищевая добавка Е526 в пищепроме: регулятор кислотности и вязкости, отвердитель, консервант. Используется при изготовлении соков и напитков, кондитерских и мучных изделий, маринадов, соли, детского питания. Применяется в сахарном производстве.
— В стоматологии известковое молоко используют для дезинфекции корневых каналов.
— Для лечения кислотных ожогов — в медицине.
— В сельском хозяйстве: средство для регулирования рН почв; в качестве натурального инсектицида от клещей, блох, жуков; для приготовления популярного фунгицида «бордосская жидкость»; для побелки стволов деревьев от вредителей и солнечных ожогов; как антимикробный и противогрибковый препарат для хранения овощей на складах; как минеральное удобрение.
— Гидроокись кальция снижает электросопротивление почвы, поэтому ею обрабатывают грунт при установке заземления.
— Хим.реактив используется при производстве эбонита, тормозных накладок, кремов для эпиляции.
ПОКАЗАТЕЛИ
| Наименование | Показатель |
| Температура плавления, оС | 512 |
| Массовая доля основного вещества, % | 98 |
| Массовая доля СаО, % | 74,50 |
| Массовая доля MgO, % | 0,60 |
| Массовая доля SiO2, % | 0,12 |
| Массовая доля Al2O3, % | 0,08 |
| Массовая доля Fe2O3, % | 0,05 |
| Массовая доля Mn3O4, % | 0,02 |
| Массовая доля S, % | 0,01 |
КАЛИЙ ГИДРОКСИД
Калий гидроксид (калий гидроокись, едкий калий) — неорганическое соединение с химической формулой КОН. Бесцветные, очень гигроскопичные кристаллы, но гигроскопичность меньше, чем у гидроксида натрия.
СВОЙСТВА
Калий гидроксид — сильная щелочь, которая получила свое название за способность разрушать органические материалы, такие как древесина, бумага, белковые и жировые ткани.
Калий гидроксид — бесцветный порошок, состоящий из чешуек или мелких кристаллов. Запаха не имеет, очень гигроскопичный. На воздухе кристаллы быстро «оплывают», поэтому хранить вещество необходимо в герметично укупоренной таре. Реактив хорошо растворяется в воде, спиртах. Активно вступает в реакции с металлами, кислотными оксидами и газами, органическими и неорганическими кислотами, органическими соединениями.
Калиевая щелочь негорюча и взрывобезопасна, но опасна для человека. При попадании на кожу или в глаза вызывает долго незаживающие ожоги и даже потерю зрения, поэтому работать с ней допускается только в резиновых перчатках, прорезиненном костюме и специальных очках, защищающих от случайных брызг опасного реактива.
Калий гидроксид способен разрушать стекло (растворы) и фарфор (расплавы). Хранят и транспортируют растворы и твердое вещество в стальных емкостях или полиэтиленовых мешках.
Калиевую щелочь получают гидролизом хлорида калия.
Гидроксид калия выпускается как в виде растворов, так и в твердой форме (хлопья, гранулы).
ПРИМЕНЕНИЕ
— В косметике применяется для получения жидкого и мягкого мыла, шампуней, мыльных кремов и отбеливателей.
— В химической промышленности — в органическом и неорганическом синтезе; как сырье для получения соединений калия (например, двуокиси калия, перманганата калия), красителей; в качестве катализатора; в производстве удобрений и пестицидов, инсектицидов, гидроокиси циркония, метана, искусственного каучука; для осушения жидкостей, а также газов, с которыми KOH не вступает в реакцию.
— Поглощение кислых газов (углекислоты, сероводорода, диоксида серы).
— В лабораторной практике калиевая щелочь используется в титровании для обнаружения некоторых катионов, для определения концентрации кислот; для нейтрализации кислот.
— Обработка целлюлозы в производстве синтетических волокон; используется для придания хлопковым тканям лучшей впитываемости.
— В качестве пеногасителя на предприятиях производства бумаги.
— В резиновой промышленности — для обработки крошки каучука.
— В пищевой индустрии — в качестве регулятора кислотности (добавка Е 525) при изготовлении шоколада и шоколадных изделий; для обработки замороженного картофеля; для чистки овощей, корнеплодов и фруктов, в том числе для детского питания.
— В электротехнике хим. реактив применяют в щелочных аккумуляторах и в алкалиновых батарейках.
— В нефтехимии — для приготовления буровых растворов; в перегонке нефти.
— Для выщелачивания отливок на сталелитейных предприятиях.
— Используется для регулирования рН, очистки сточных вод.
— В промышленной очистке изделий из нержавеющей стали от жиросодержащих загрязнений, следов механической обработки.
— В быту — входит в состав средств для мытья нержавейки.
— Для ресомации (метод аналогичный кремации, но на химической основе).
— Применяется для травления кристаллов кремния в микроэлектронике.
— В фармацевтике, стоматологии, медицине (нейтрализация кислотных ожогов).
— В строительстве — при изготовлении штукатурок, побелок, гипсовых растворов.
ПОКАЗАТЕЛИ
| Наименование | Показатель | ||||
| чистый | чистый для анализа | химически чистый | марка А | марка Б | |
| Внешний вид | чешуйки белого цвета | чешуйки от белого до серого | |||
| Массовая доля гидроокиси калия (КОН), %, не менее | 84,5 | 85 | 86 | 90 | 90 |
| Массовая доля углекислого калия (К2СО3), %, не более | 1,5 | 1 | 0,6 | 0,5 | 0,5 |
| Массовая доля хлоридов, %, не более | 0,008 | 0,004 | 0,002 | 0,01 | 0,01 |
| Массовая доля железа (Fe), %, не более | 0,001 | 0,0005 | 0,0005 | 0,0003 | 0,0003 |
| Массовая доля натрия в пересчете на NaOH, не более | — | — | — | 1 | 1 |
| Массовая доля сульфатов (SO4), %, не более | 0,003 | 0,002 | 0,0005 | 0,005 | 0,005 |
| Массовая доля нитратов и нитритов в пересчете на азот (N), %, не более | 0,001 | 0,0005 | 0,0005 | 0,0005 | 0,0005 |
| Массовая доля никеля, %, не более | 0,001 | 0,01 | |||
| Массовая доля кремнекислоты (SiO2), %, не более | 0,005 | 0,002 | 0,002 | 0,0005 | 0,0005 |
| Массовая доля фосфатов (РО4), %, не более | 0,001 | 0,0002 | 0,0002 | 0,0002 | 0,0002 |
| Массовая доля тяжелых металлов (Ag), %, не более | 0,001 | 0,0005 | 0,0005 | 0,0005 | 0,0005 |
| Массовая доля алюминия (Al), %, не более | 0,001 | 0,0001 | 0,0001 | 0,0001 | 0,0001 |
| Массовая доля (Са), %, не более | 0,001 | 0,001 | 0,001 | 0,001 | 0,001 |
ЭРИОХРОМ ЧЕРНЫЙ Т
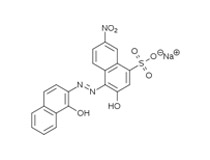
Эриохром чёрный Т — органическое соединение, прямой азокраситель. Черные кристаллы, дающие водные растворы, цвет которых зависит от кислотности.
СВОЙСТВА
В нормальных условиях представляет собой темно-коричневые или черные кристаллы с легким запахом. В воде растворяется плохо, в спирте хорошо. Не горюч, токсичен. Один из самых часто применяемых в аналитической химии индикаторов на сегодняшний день для определения катионов и анионов.
Эриохром черный Т вступает с катионами марганца, цинка, магния, кадмия, ртути (II), свинца (II) и еще несколькими катионами в обратимые цветные реакции. Чистый водный раствор ализаринхромового черного при показателе кислотности рН 6 винно-красный, при возрастании рН от 8 до 12 — темно-синий, и становится оранжевым рН 13.
При работе с веществом необходимо использовать химзащитные перчатки, респиратор, защитные очки с боковой защитой. Стараться, чтобы вещество не попадало на одежду, по возможности использовать специальный защитный костюм. Работы должны проводиться в помещении с хорошей вентиляцией. При попадании на кожу или в глаза промыть большим количеством воды и обратиться к врачу. При проглатывании срочно обратиться к врачу!
Эриохром чёрный Т хранят в плотно закрытой таре в сухих помещениях. Оптимальная температура хранения от +5 до +25 °C. Утилизация реактива и тары, в которой он хранился, производится по правилам утилизации опасных отходов.
ПРИМЕНЕНИЕ
В основном эриохром черный Т применяется для определения жесткости воды методом комплексометрического титриметрического анализа. Он может использоваться для этих целей как в виде раствора, так и в виде компонента сухой смеси. Для изготовления смеси 0,5 г реактива растворяют в 10 см3 буферного раствора, наливают 90 см3 этилового спирта и смешивают. Хранят раствор в холодильном шкафу, в закрытой таре до 2 месяцев.
Для изготовления сухой смеси 0,5 г индикатора растирают вместе с 50 г хлористого натрия в ступке. Смесь можно хранить до года в закрытой таре из темного стекла.
Титрование с ЕВТ эффективно для определения содержание катионов кальция, магния и железа.
ПОКАЗАТЕЛИ
| Наименование | Показатель |
| Внешний вид | Черный или коричневый порошок |
| Массовая доля основного вещества, %, не менее | 85,0 |
| Массовая доля остатка после прокаливания, %, не более | 10 |
| Потери при высушивании, % | 2,0 |
| Оптическая плотность водного раствора, не более | 1,35-1,65 |
| Вода, %, не более | 4,5 |
ФЕНОЛФТАЛЕИН
Фенолфталеин — трифенилметановый краситель, кислотно-основный индикатор, изменяющий окраску от бесцветной (при рН < 8,2) до красно-фиолетовый, «малиновой» (в щелочной); но в концентрированной щелочи — вновь бесцветен. В концентрированной серной кислоте образует розовый катион.
СВОЙСТВА
Фенолфталеин (лекарственный препарат – пурген, лаксатол) представляет собой сложное химическое соединение органического происхождения, имеющее форму бесцветных, иногда со слабо-желтым оттенком, кристаллов в виде ромбов, без определенного вкуса, но со специфическим запахом. Оно хорошо растворятся в диэтиловом эфире, спирте, но плохо – в воде. Данный химический реактив получается путем реакции между фенолом (карболовая кислота) и фталевым ангидридом в соединении с серной кислотой. В настоящее время данный химреактив широко применяется как в аналитической химии, фармакологии, так и в медицине.
Фенолфталеин относится ко второму классу опасности химических веществ, поэтому при его хранении и транспортировке требуется соблюдение особых мер безопасности. Учитывая свойства данного химреактива вызывать кожные реакции, при работе с ним необходимо использовать средства защиты, такие как перчатки нитриловые или перчатки смотровые, фартуки, бахилы, защитные маски.
Хранить данное химическое соединение необходимо в специальной лабораторной посуде из стекла, а осуществлять перевозку – в специальных цистернах из нержавеющей стали. Срок годности в виде сухого вещества неограничен, в спиртовом растворе – не более одного месяца.
ПРИМЕНЕНИЕ
Фенолфталеин применяется в различных областях:
— химия. Трудно представить химический арсенал современной лаборатории без такого сложного вещества как фенолфталеин. Это обусловлено его способностью изменять окраску вещества или среды в зависимости от его кислотности. Благодаря этому свойству при работы с химическими реактивами определяется их уровень кислотности и щелочности. Поэтому, основное применение фенолфталеина в практической химии – как кислотно-основной индикатор для слабых кислот:
— сильнокислая (оранжевый);
— слабокислая и нейтральная (бесцветный);
— щелочная (розовый, сиреневый, пурпурный);
— сильнощелочная (бесцветный).
Кроме того, как дополнительный компонент, фенолфталеин входит в состав многих смешанных индикаторов, которые используются для определения уровня кислотности буферных и без буферных растворов. Большое применение он также нашел в аналитической химии в процессе титрования водных растворов, а также при качественном анализе многих химических элементов, например, кадмия, цинка, свинца и магния, при опрыскивании которых изменяется окраска;
— медицина. В настоящее время фенолфталеин, как и много десятилетий назад, применяется в качестве слабительного средства при хронических запорах. Однако последние исследования доказали наличие в данном химическом препарате карценогенов. По этой причине во многих странах мира пурген запрещен как медицинский препарат. А в странах, где все же его применение допустимо, существует ряд ограничений на его использование: применение с особой осторожностью в крайне особых случаях. Категорически запрещен в период беременности, детям и пожилым людям, а также больным с проблемами мочевыводящей системы. Кроме того, он полностью отменен в свободной продаже как аптечный препарат.
ПОКАЗАТЕЛИ
| Наименование | Показатель |
| Внешний вид | Белый порошок, без запаха |
| Интервал перехода окраски, рН, в пределах | 8,2-10 |
| Температура плавления, оС, в пределах | 258 — 263 |
| Массовая доля остатка после прокаливания, %, не более | 0,05 |
МЕТИЛОВЫЙ ОРАНЖЕВЫЙ
Метиловый оранжевый — известный кислотно-основный индикатор, синтетический органический краситель из группы азокрасителей, является солью натрия.
СВОЙСТВА
Метилоранж относится к группе органических красителей, способных изменять свою окраску в водном растворе при изменении рН среды от красного цвета до оранжево-жёлтого.
Так, например, в кислой среде он приобретает красный цвет, в нейтральной – оранжевый, в щелочной — оттенки жёлтого.
На интервал перехода окраски могут повлиять такие факторы, как:
— температура (оказывает наибольшее влияние),
— наличие или отсутствие в растворе органических растворителей, солей, белковых веществ и других.
Влияние температуры наиболее значительно для индикаторов, являющихся слабыми основаниями: например, для метилового оранжевого при комнатной температуре окраска изменяется в пределах рН 3,1-4,4, а при 100°С — в пределах рН 2,5-3,7.
Переход окраски в водных растворах от красной к оранжево-жёлтой наблюдается в области рН 3,1-4,4 (в кислой среде красный, в щелочной — жёлтый).
Токсичен.
ПРИМЕНЕНИЕ
Сфера применения индикаторов очень обширна. Они используются:
— для определения содержания кислот и щелочей в различных растворах, а также кислотности желудочного сока;
— для колориметрического метода измерения интенсивности окраски и определения рН биологических жидкостей;
— для определения водородного показателя (pH) среды.
Для всех вышеуказанных целей метилоранж, как и другие индикаторы, применяют в виде:
— спиртовых или водных растворов;
— специальных индикаторных бумажек (фильтровальная бумага, пропитанная растворами индикаторов).
Кроме того, благодаря своим особым химическим свойствам метилоранж, как кислотный анионный краситель, используется в современной текстильной промышленности при крашении шерсти, нейлона и шелка.
ПОКАЗАТЕЛИ
| Наименование | Показатель |
| Внешний вид | Кристаллический порошок оранжевого цвета |
| Максимум кривой светопоглощения, 0,0005% раствор, нм | 505 ± 5 |
| Оптическая плотность 0,0005 % раствора в макс. кривой светопоглощения, нм, не менее | 0,65 |
| Интервал pH перехода окраски от красной к желтой | 3,0-4,4 |
| Нерастворимые в воде вещества, %, не более | 0,1 |
| Массовая доля остатка после прокаливания, %, не более | 19-22 |
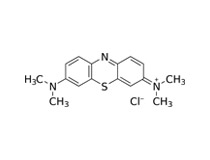
МЕТИЛЕНОВЫЙ СИНИЙ (ГОЛУБОЙ)
Метиленовый синий — краситель. Представляет собой тёмно-зеленые кристаллы с бронзовым блеском.
СВОЙСТВА
Малорастворим в воде, этаноле, практически нерастворим в диэтиловом эфире и хлороформе. Легко восстанавливается: E0 = +0,53 В. В водных растворах мономерная форма поглощает свет при длине волны λmax = 668 нм, димер — в λmax = 612 нм; константа димеризации Кдим = 5,00⋅103 (pH 4—5,5).
ПРИМЕНЕНИЕ
Органический основной тиазиновый краситель, применяется для окраски хлопка, шерсти и шёлка в ярко-голубой цвет, однако краска разрушается на свету. В аналитической химии применяется для определения хлоратов, перхлоратов, катионов ртути, олова, магния, кальция, кобальта, кадмия.
В медицине используется в качестве антисептика для лечения инфекций ротовой полости и мочеполовых путей. Относится к списку жизненно важных препаратов ВОЗ для лечения метгемолгобинемии (антидот при отравлении цианидами, угарным газом и сероводородом). Имеются сообщения о высокой эффективности этого соединения при лечении болезни Альцгеймера.
Используют в микроскопии как красящее вещество, так как метиленовый синий интенсивно окрашивает некоторые ткани живого организма.
В аквариумистике применяется довольно часто во время инкубирования икры в качестве антисептика.
В водоочистке применяется при тестировании активированного угля.
В фотографии может использоваться как десенсибилизатор в значительном разведении. В высокой концентрации вместо десенсибилизирующего действия оказывает вуалирование.
ПОКАЗАТЕЛИ
| Наименование | Показатель |
| Внешний вид | Синий гомогенный порошок |
| Массовая доля основного вещества, % | 100 |
| Потери при высушивании, % | ≤ 14 |
| Железо, ppm | ≤ 300 |
| Цинк, ppm | ≤ 150 |
| Свинец, ppm | ≤ 1 |
| Мышьяк, ppm | ≤ 0.5 |
БРОМФЕНОЛОВЫЙ СИНИЙ
Бромфеноловый синий — натуральный краситель, также применяемый в лабораторной практике как рН-индикатор и маркёр при проведении электрофореза.
СВОЙСТВА
Легко растворим в воде. Переход окраски раствора от желтой к синей в интервале рН 3,0—4,6.
ПРИМЕНЕНИЕ
Применяется как индикатор при электрофорезе нуклеиновых кислот или белка в агарозе или полиакриламид-геле.
ПОКАЗАТЕЛИ
| Наименование | Показатель |
| Агрегатное состояние при 20 °C | Твердое |
| Цвет | Бледно-оранжевый |
| Запах | Без запаха |
| Температура плавления, °C | 273 |
| Температура кипения, °C | 279 |
| Растворимость в воде [% вес] | 0,4 / 100 при 20 °C |
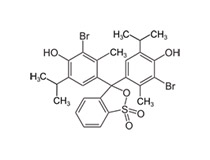
БРОМТИМОЛОВЫЙ СИНИЙ
Бромтимоловый синий — трифенилметановый краситель, малорастворимый в воде, кислотно-основный индикатор.
СВОЙСТВА
Бромтимоловый синий (дибромтимолсульфофталеин) — составной трифенилметановый краситель, который сложно растворить в воде, выполняет функцию кислотно-основного индикатора. Простыми словами: индикатор для pH среды, в нашем случае – воды. Бромтимоловый синий различает значения pH в диапазоне показаний от 5,8 до 7,6, отображая это изменением цвета с желтого к синему, становясь зеленоватым при средних показаниях. Нейтральные значения pН, а именно 7,0, создают травянисто-зелёный цвет у раствора.
ПРИМЕНЕНИЕ
В аналитической химии бромтимоловый синий применяется в кислотно-основном титровании и для определения нейтрального значения водородного показателя (pH=7,0) при титровании (приобретает травянисто-зелёный оттенок).
Бромтимоловый синий применяется в бактериологии как краситель в составе питательной среды, а также в качестве фотосенсибилизатора в копировальной технике.
Существует несколько способов приготовить рабочий раствор индикатора на основе бромтимолового синего:
— 1 % раствор бромтимолового синего в диметилформамиде;
— 0,04 г. бромтимолового синего в 0,64 мл 0,1-молярного раствора едкого натра и разбавить раствор 100 мл свежепрокипячённой охлаждённой воды.
ПОКАЗАТЕЛИ
| Наименование | Показатель |
| Внешний вид | Мелкокристаллический порошок розовато-фиолетового цвета |
| Интервал визуального перехода, рН | 6,0 (желтый) – 7,6 (голубой) |
| Индекс абсорбции L/CM.G | 55,0 |
| Растворимость в этаноле | соответствует |
| Остаток после прокаливания,% | 0,02 |